nur für Forschungszwecke
Molidustat (BAY 85-3934) HIF Modulator
Kat.-Nr.S8138
-chemical-structure-s8138.gif)
Chemische Struktur
Molekulargewicht: 314.30
Qualitätskontrolle
| Verwandte Ziele | EGFR VEGFR JAK PDGFR FGFR Src FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Weitere HIF Inhibitoren | PT2399 PX-478 Dihydrochloride BAY 87-2243 KC7F2 Lificiguat (YC-1) IOX2 CAY10585 (LW 6) PT2385 IDF-11774 MK-8617 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 314.30 | Formel | C13H14N8O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1154028-82-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1COCCN1C2=NC=NC(=C2)N3C(=O)C(=CN3)N4C=CN=N4 | ||
Löslichkeit
|
In vitro |
DMSO
: 10 mg/mL
(31.81 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PHD2
(Cell-free assay) 280 nM
PHD3
(Cell-free assay) 450 nM
PHD1
(Cell-free assay) 480 nM
|
|---|---|
| In vitro |
In vitro induziert Molidustat (BAY 85-3934) die Transkription von Hypoxie-sensitiven Genen in HeLa-, A549- und Hep3B-Zellen. |
| Kinase-Assay |
Prolylhydroxylase-Assay
|
|
Biotinyliertes HIF-1α 556–574 (biotinyl-DLDLEMLAPYIPMDDDFQL) wird an weiße 96-Well-NeutrAvidin-Platten mit hoher Bindungskapazität gebunden, die mit Blocker Casein vorblockiert und anschließend mit 1 mM Biotin blockiert werden. Das immobilisierte Peptidsubstrat wird mit der entsprechenden Menge HIF-PH in einem Puffer inkubiert, der 20 mM Tris (pH 7,5), 5 mM KCl, 1,5 mM MgCl2, 20 µM 2-Oxoglutarat, 10 µM FeSO4, 2 mM Ascorbat, 4 % Proteaseinhibitoren ohne EDTA in einem Endvolumen von 100 µl enthält, mit oder ohne Molidustat (BAY 85-3934), das in geeigneten Konzentrationen zugesetzt wird. Die Reaktionszeit beträgt 60 min. Um die Reaktion zu stoppen, werden die Platten dreimal mit Waschpuffer gewaschen. Hydroxyliertes biotinyl-HIF-1α 556–574 wird mit Eu-VBC in 100 µl Bindungspuffer (50 mM Tris [pH 7,5], 120 mM NaCl) für 60 min bei Raumtemperatur inkubiert. Nach sechsmaligem Waschen mit DELFIA-Waschpuffer und Zugabe von 100 µl Enhancer-Lösung wird die Menge des gebundenen VBC durch Messung der zeitaufgelösten Fluoreszenz mit einem Tecan Infinite M200 Plattenlesegerät bestimmt. Die Messungen werden dreifach oder mehr durchgeführt, und die Ergebnisse werden als Mittelwerte ± SEM ausgedrückt. IC50-Werte für diese Verbindung werden nach Kurvenanpassung mittels GraphPad Prism Software unter Anwendung der Vier-Parameter-Logistikgleichung auf die Datensätze bestimmt.
|
|
| In vivo |
Bei gesunden Wistar-Ratten und Cynomolgus-Affen induziert Molidustat (BAY 85-3934) (1,5 mg/kg, p.o.) eine dosisabhängige Produktion von EPO und Erythropoese. Bei Ratten mit induzierter renaler Anämie ist diese Verbindung (5 mg/kg, p.o.) auch wirksam bei der Erhöhung des Hämatokritspiegels, während sie die endogene EPO-Produktion ohne hypertensive Effekte stimuliert. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | HIF-1α |
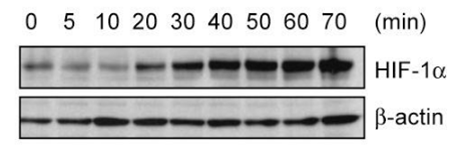
|
25392999 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03418168 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
February 22 2018 | Phase 3 |
| NCT03351166 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
January 22 2018 | Phase 3 |
| NCT03350347 | Completed | Anemia|Renal Insufficiency Chronic |
Bayer |
December 13 2017 | Phase 3 |
| NCT02312973 | Completed | Renal Insufficiency Chronic |
Bayer |
January 14 2015 | Phase 1 |
| NCT01458028 | Completed | Anemia |
Bayer |
September 2011 | Phase 1 |
| NCT01332942 | Completed | Anemia |
Bayer |
April 2011 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
