nur für Forschungszwecke
RITA p53 Aktivator
Kat.-Nr.S2781
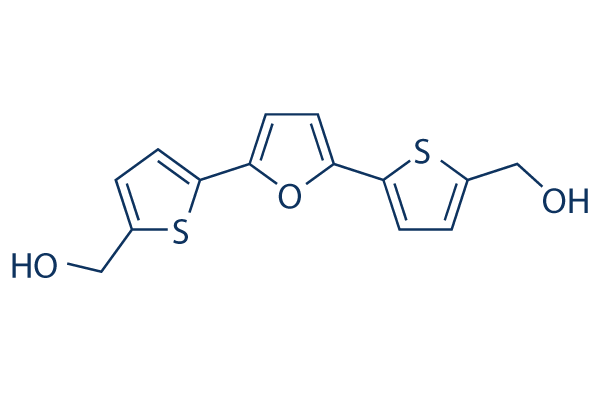
Chemische Struktur
Molekulargewicht: 292.37
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 292.37 | Formel | C14H12O3S2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 213261-59-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | NSC 652287 | Smiles | C1=C(SC(=C1)C2=CC=C(O2)C3=CC=C(S3)CO)CO | ||
Löslichkeit
|
In vitro |
DMSO
: 58 mg/mL
(198.37 mM)
Ethanol : 8 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Inducer of DNA cross-links, not a DNA intercalator.
|
|---|---|
| Targets/IC50/Ki |
Mdm2
p53
|
| In vitro |
RITA zeigt ein hochselektives Muster differentieller zytotoxischer Aktivität in den Tumorzelllinien, aufgrund zellulärer Akkumulation in der zytosolischen (S100) Fraktion. Diese Verbindung hemmt auch das Wachstum anderer Nierenzelllinien, einschließlich ACHN und UO-31, mit IC50-Werten von 13 μM bzw. 37 μM. Es (10 nM) verursacht einen Zellzyklusarrest mit Akkumulation von Zellen in der G2-M-Phase und induziert DNA-Fragmentierung und Apoptosis bei 100 nM, beides mit erhöhten p53-Proteinspiegeln. Diese Chemikalie (30 nM) induziert auch DNA-Protein- und DNA-DNA-Quervernetzungen in A498-Zellen. Gleichzeitig hat sie keine Auswirkungen auf die Top1-vermittelte Entspannung von supercoiled SV40-DNA. Es unterdrückt das Wachstum von HCT116-Zellen signifikant (97%), hemmt aber nur geringfügig das Wachstum von HCT116 TP53-/--Zellen (13%). Diese Verbindung ist bei der Wachstumsunterdrückung in Tumorzelllinien, die Wildtyp-p53 exprimieren, wesentlich effizienter als in Zelllinien, denen p53 fehlt, und solchen, die mutiertes p53 exprimieren. Es bindet volllängiges p53, aber nicht Glutathion-S-Transferase (GST)-Protein oder HDM-2 (ein Schlüsselregulator von p53 wird durch die Rettung der embryonalen Letalität von MDM2 stark unterstützt). Diese Chemikalie blockiert die p53−HDM-2-Interaktion und die p53-Ubiquitinierung. Es verringert die Menge an HDM-2, die mit p53 co-präzipitiert wird, erheblich, obwohl beide Proteine hochreguliert sind. Diese Verbindung verhindert Interaktionen zwischen den gereinigten GST-p53- und 6XHis-getaggten His-HDM-2-Proteinen. Es wird gezeigt, dass es Apoptosis durch Förderung der p53Ser46-Phosphorylierung induziert. Diese Chemikalie induziert die Aktivierung von p53 in Verbindung mit der Hochregulierung von phosphoryliertem ASK-1, MKK-4 und c-Jun. Es induziert die Aktivierung der JNK-Signalübertragung. Im Gegensatz dazu zeigen jedoch andere Ergebnisse mittels Kernspinresonanz (NMR), dass es die Bildung des Komplexes zwischen p53 (Reste 1-312) und der N-terminalen p53-bindenden Domäne von MDM2 (Reste 1-118) nicht blockiert, was sehr wahrscheinlich darauf hindeutet, dass die Bindung dieser Verbindung eine native Konformation von p53 erfordert.
|
| In vivo |
RITA wird Mäusen nach intraperitonealer Verabreichung gut vertragen, ohne dass bei Dosen von bis zu 10 mg/kg über einen Monat lang ein Gewichtsverlust zu beobachten war. Nach fünf Injektionen von 0,1 mg/kg dieser Verbindung wird das Wachstum der HCT116-Tumoren um 40% unterdrückt, ohne offensichtliche Auswirkungen auf die HCT116 TP53-/--Tumoren. Bei einer Dosis von 1 oder 10 mg/kg zeigt es eine starke Antitumoraktivität. Fünf 1 mg/kg-Injektionen dieser Chemikalie führen zu einer mehr als zweifachen Verringerung der Wachstumsrate von p53-positiven Xenografts ohne Auswirkungen auf p53-negative Xenografts. HCT116-Tumoren sind bei Mäusen, die mit 10 mg/kg davon behandelt wurden, um 90% kleiner als bei unbehandelten Kontrollmäusen. Diese Verbindung hemmt das Tumorwachstum auf eine Wildtyp-p53-abhängige Weise.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05260203 | Completed | Multiple Myeloma|Solitary Plasmacytoma|Amyloidosis|Chronic Myeloid Leukemia|Chronic Lymphocytic Leukemia|T Cell Non-Hodgkin Lymphoma|Lymphocytic Lymphoma|Hodgkin Lymphoma|B-cell Non Hodgkin Lymphoma|Acute Myeloid Leukemia|Myelodysplasia|Chronic Myeloproliferative Disorder|Treatment Adherence|Treatment Adherence and Compliance |
Advice Pharma Group srl |
June 4 2022 | Not Applicable |
| NCT05153551 | Completed | Autism Spectrum Disorder |
University of Michigan|Blue Cross Blue Shield of Michigan Foundation |
January 27 2022 | Not Applicable |
| NCT03806127 | Completed | Irritable Bowel Syndrome |
Urovant Sciences GmbH |
December 31 2018 | Phase 2 |
| NCT00779025 | Completed | Coitus |
Johnson & Johnson Consumer and Personal Products Worldwide |
January 2008 | Not Applicable |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
