nur für Forschungszwecke
SAR-020106 Chk Inhibitor
Kat.-Nr.S7740
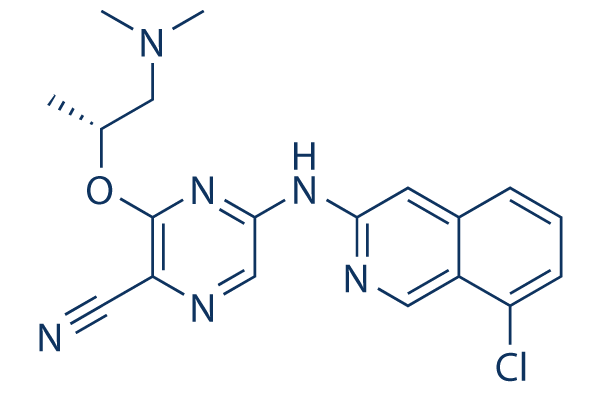
Chemische Struktur
Molekulargewicht: 382.85
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HT-29 cells | Function assay | Antimitotic activity in etoposide-induced human HT-29 cells assessed as induction of M-phase phosphoprotein 2 expression by ELISA, IC50=0.055 μM | ||||
| HEK cells | Function assay | Inhibition of human ERG overexpressed in HEK cells, IC50=5 μM | ||||
| SW620 cells | Function assay | Inhibition of CHK1 in human SW620 cells assessed as potentiation of gemcitabine-induced cytotoxicity after 24 to 48 hrs | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 382.85 | Formel | C19H19ClN6O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1184843-57-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC(CN(C)C)OC1=NC(=CN=C1C#N)NC2=NC=C3C(=C2)C=CC=C3Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 20 mg/mL
(52.23 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Chk1
(Cell-free assay) 13.3 nM
|
|---|---|
| In vitro |
SAR-020106 hebt einen Etoposid-induzierten G2-Arrest mit einer IC50 von 55 nmol/L in HT29-Zellen auf und verstärkt die Abtötung von Gemcitabin und SN38 durch Zellen um das 3,0- bis 29-fache in mehreren Kolontumorlinien in vitro und p53-abhängig. Diese Verbindung hemmt die zytotoxische medikamenteninduzierte Autophosphorylierung von CHK1 an S296 und blockiert die Phosphorylierung von CDK1 an Y15 dosisabhängig.
|
| In vivo |
SAR-020106 kann die Antitumorwirkung von Irinotecan und Gemcitabin in vivo mit entsprechenden Biomarkeränderungen und minimaler Toxizität verstärken. Obwohl die orale Bioverfügbarkeit bei Mäusen minimal ist (F = 5 %), war die Verteilung dieser Verbindung nach i.p. Dosierung (40 mg/kg) ausreichend, um CHK1 in den Tumoren zu hemmen, wie durch die Hemmung der Irinotecan-induzierten CHK1 pS296-Autophosphorylierung gezeigt wurde. Bei Dosen, die eine Hemmung der CHK1-Aktivität in vivo bewirken, zeigte diese Verbindung keine Einzelwirkstoffaktivität im SW620-Xenograft-Modell, und die Tumoren wuchsen mit ähnlichen Raten wie die vehikelbehandelten Kontrollen. Bei der Dosierung (i.p.) in Kombination mit Irinotecan wurde beobachtet, dass diese Verbindung die Antitumoraktivität des genotoxischen Arzneimittels im SW620-Xenograft-Modell potenzierte.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
