nur für Forschungszwecke
CYC116 Aurora Kinase Inhibitor
Kat.-Nr.S1171
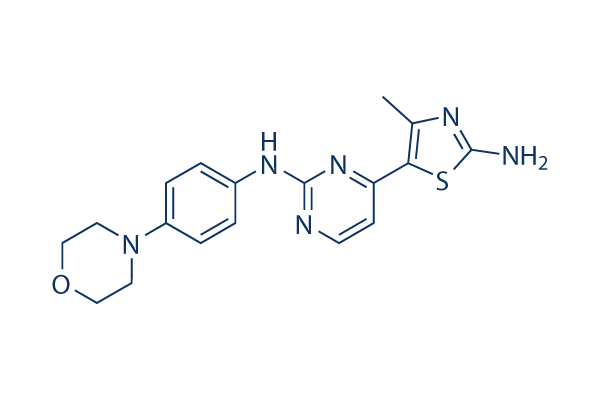
Chemische Struktur
Molekulargewicht: 368.46
Qualitätskontrolle
| Verwandte Ziele | CDK HSP PD-1/PD-L1 ROCK Wee1 DNA/RNA Synthesis Microtubule Associated Ras KRas Casein Kinase |
|---|---|
| Weitere Aurora Kinase Inhibitoren | Hesperadin Barasertib-HQPA (AZD2811) Alisertib (MLN8237) Tozasertib (VX-680) ZM 447439 MLN8054 Danusertib (PHA-739358) MK-5108 TCS7010 (Aurora A Inhibitor I) AMG-900 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| A2780 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human A2780 cells after 96 hrs by MTT assay | |||
| MIAPaCa2 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human MIAPaCa2 cells after 96 hrs by MTT assay | |||
| HT-29 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human HT-29 cells after 96 hrs by MTT assay | |||
| MCF7 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human MCF7 cells after 96 hrs by MTT assay | |||
| HeLa cells | Cytotoxicity assay | 96 h | Cytotoxicity against human HeLa cells after 96 hrs by MTT assay | |||
| COLO205 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human COLO205 cells after 96 hrs by MTT assay | |||
| HCT116 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human HCT116 cells after 96 hrs by MTT assay | |||
| K562 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human K562 cells after 96 hrs by MTT assay | |||
| CCRF-CEM cells | Cytotoxicity assay | 96 h | Cytotoxicity against human CCRF-CEM cells after 96 hrs by MTT assay | |||
| MV4-11 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human MV4-11 cells after 96 hrs by MTT assay | |||
| HL60 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human HL60 cells after 96 hrs by MTT assay | |||
| NCI-H460 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human NCI-H460 cells after 96 hrs by MTT assay | |||
| MESSA cells | Cytotoxicity assay | 96 h | Cytotoxicity against human MESSA cells after 96 hrs by MTT assay | |||
| U2OS cells | Function assay | 0.07-10 uM | 2 h | Inhibition of Aurora kinase in nocodazole-synchronized human U2OS cells assessed as reduction of histone H3 serine-10 phosphorylation at 0.07 to 10 uM after 2 hrs immunofluorescence microscopy | ||
| A549 cells | Function assay | 0.5-2 μM | 7 h | Cell cycle arrest in asynchronous human A549 cells assessed as accumulation of cyclin B1-negative tetraploid cells at G1 phase at 0.5 to 2 uM after 7 hrs by FACS analysis | ||
| SW620 cells | Function assay | 1 μM | 48 h | Effect on mitotic index in human SW620 cells assessed as appearance of polyploid cells at 1 uM after 48 hrs by propidium iodide staining-based FACS analysis | ||
| HeLa cells | Function assay | 1.25 μM | 7 h | Inhibition of Aurora kinase in human HeLa cells assessed as complete inhibition of histone H3 phosphorylation at 1.25 uM after 7 hrs by Western blot analysis | ||
| A549 cells | Function assay | 7 h | Inhibition of Aurora kinase in human A549 cells assessed as concentration required for half-maximal inhibition of histone H3 serine-10 phosphorylation after 7 hrs immunofluorescence microscopy | |||
| BxPC3 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human BxPC3 cells after 96 hrs by MTT assay | |||
| HUPT4 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human HUPT4 cells after 96 hrs by MTT assay | |||
| Saos2 cells | Cytotoxicity assay | 96 h | Cytotoxicity against human Saos2 cells after 96 hrs by MTT assay | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 368.46 | Formel | C18H20N6OS |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 693228-63-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(SC(=N1)N)C2=NC(=NC=C2)NC3=CC=C(C=C3)N4CCOCC4 | ||
Löslichkeit
|
In vitro |
DMSO
: 24 mg/mL
(65.13 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
An orally bioavailable, small molecule inhibitor of Aurora kinase/VEGFR2.
|
|---|---|
| Targets/IC50/Ki |
Aurora A
(Cell-free assay) 8 nM(Ki)
Aurora B
(Cell-free assay) 9 nM(Ki)
VEGFR2
(Cell-free assay) 44 nM(Ki)
FLT3
(Cell-free assay) 44 nM(Ki)
CDK2/CyclinE
(Cell-free assay) 0.39 μM(Ki)
CDK9/CyclinT
(Cell-free assay) 0.48 μM(Ki)
p70 S6K
(Cell-free assay) 0.54 μM(Ki)
|
| In vitro |
Das am stärksten Aurora-selektive CYC116 zeigt eine hemmende Wirkung auf Aurora A- und B-Kinasen, die 50-fach potenter ist als jede der getesteten CDKs. Diese Verbindung wird anfänglich gegen eine Reihe von menschlichen Leukämie- und soliden Tumorzelllinien mittels eines MTT-Antiproliferationsassays gescreent. Die Ergebnisse zeigen, dass sie eine breitspektrale Antitumoraktivität besitzt und eine spezifische Zytotoxizität gegen die akute myeloische Leukämie-Zelllinie MV4-11 mit einer IC50 von 34 nM aufweist. Darüber hinaus wird festgestellt, dass die antiproliferative Aktivität dieser Chemikalie mit der Modulation von Aurora A und B verbunden ist, wie z.B. der Hemmung der Aurora-Autophosphorylierung, der Reduktion der Histon-H3-Phosphorylierung, der Polyploidie, gefolgt von Zelltod, resultierend aus einem Versagen der Zytokinese.
|
| Kinase-Assay |
Kinase-Assays
|
|
Aurora A Kinase-Assays werden mit einem Reaktionsvolumen von 25 μL (25 mM β-Glycerophosphat, 20 mM Tris/HCl, pH 7,5, 5 mM EGTA, 1 mM DTT, 1 mM Na3VO4, 10 μg Kemptid (Peptidsubstrat)) durchgeführt. Rekombinante Aurora A Kinase wird in 20 mM Tris/HCl, pH 8, verdünnt, das 0,5 mg/mL BSA, 2,5% Glycerin und 0,006% Brij-35 enthält. Die Reaktionen werden durch Zugabe von 5 μL Mg/ATP-Mix (15 mM MgCl2, 100 μM ATP, mit 18,5 kBq γ-32P-ATP pro Well) gestartet und 30 Minuten bei 30°C inkubiert, bevor sie mit 25 μL 75 mM H3PO4 beendet werden. Aurora B Kinase-Assays werden wie Aurora A durchgeführt, außer dass Aurora B vor der Verwendung in einer separaten Reaktion bei 30°C für 60 Minuten mit innerem Zentromerprotein aktiviert wird.
|
|
| In vivo |
Mäuse mit subkutanen NCI-H460 Xenografts erhalten CYC116 oral über 5 Tage in Dosen von 75 und 100 mg/kg q.d. Dies führt zu einer Verzögerung des Tumorwachstums von 2,3 bzw. 5,8 Tagen, was sich in spezifischen Wachstumsverzögerungen von 0,32 bzw. 0,81 widerspiegelt.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
