nur für Forschungszwecke
MK-5108 Aurora Kinase Inhibitor
Kat.-Nr.S2770
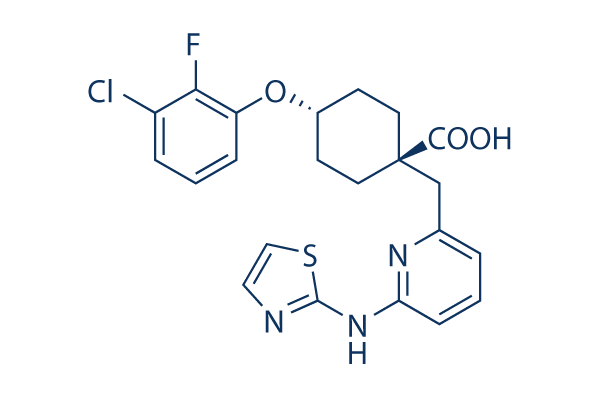
Chemische Struktur
Molekulargewicht: 461.94
Qualitätskontrolle
| Verwandte Ziele | CDK HSP PD-1/PD-L1 ROCK Wee1 DNA/RNA Synthesis Microtubule Associated Ras KRas Casein Kinase |
|---|---|
| Weitere Aurora Kinase Inhibitoren | Hesperadin Barasertib-HQPA (AZD2811) Alisertib (MLN8237) Tozasertib (VX-680) ZM 447439 MLN8054 Danusertib (PHA-739358) TCS7010 (Aurora A Inhibitor I) AMG-900 PHA-680632 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| BL21 (DE3) Rosetta | Function assay | 30 mins | Inhibition of His-tagged human Aurora A kinase (122 to 40 residues) expressed in Escherichia coli BL21 (DE3) Rosetta cells using biotinylated STK2 substrate incubated for 30 mins by HTRF assay, IC50 = 0.000064 μM. | 27391133 | ||
| HeLa Kyoto | Function assay | 20 hrs | Inhibition of Aurora A kinase autophosphorylation at Thr288 in human HeLa Kyoto cells incubated for 20 hrs, IC50 = 0.3 μM. | 27391133 | ||
| HCC1143 | Antiproliferation assay | Antiproliferation activity against human HCC1143 cells assessed as inhibition of cell proliferation, IC50 = 0.42 μM. | 28918096 | |||
| AU565 | Antiproliferation assay | Antiproliferation activity against human AU565 cells assessed as inhibition of cell proliferation, IC50 = 0.45 μM. | 28918096 | |||
| MCF7 | Antiproliferation assay | Antiproliferation activity against human MCF7 cells assessed as inhibition of cell proliferation, IC50 = 0.52 μM. | 28918096 | |||
| HCC1806 | Antiproliferation assay | Antiproliferation activity against human HCC1806 cells assessed as inhibition of cell proliferation, IC50 = 0.56 μM. | 28918096 | |||
| CAL851 | Antiproliferation assay | Antiproliferation activity against human CAL851 cells assessed as inhibition of cell proliferation, IC50 = 0.74 μM. | 28918096 | |||
| HeLa | Function assay | 16 mg/kg | 2 days | Plasma concentration in F344/N Jcl-rnu rat xenografted with luciferase expressing human HeLa cells at 16 mg/kg, po BID for 2 days, Cp = 1.7 μM. | 28918096 | |
| HeLa | Function assay | 32 mg/kg | 2 days | Plasma concentration in F344/N Jcl-rnu rat xenografted with luciferase expressing human HeLa cells at 32 mg/kg, po BID for 2 days, Cp = 4.4 μM. | 28918096 | |
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| BL21-Codon-Plus(DE3)-RIL | Function assay | 120 mins | Inhibition of human N-terminal His-tagged Aurora A expressed in Escherichia coli BL21-Codon-Plus(DE3)-RIL cells using 5-carboxy-fluorescein-y-aminobutyric acid-Ala-Leu-Arg-Arg-Ala-Ser-Leu-Gly-NH2 as substrate after 120 mins by fluorescence polarization as, IC50 = 0.00054 μM. | ChEMBL | ||
| HeLaS3 | Cytotoxicity assay | 3 days | Cytotoxicity against human HeLaS3 cells assessed as cell growth inhibition after 3 days by WST-8 assay, IC50 = 1.26 μM. | ChEMBL | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 461.94 | Formel | C22H21ClFN3O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1010085-13-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | VX-689 | Smiles | C1CC(CCC1OC2=C(C(=CC=C2)Cl)F)(CC3=NC(=CC=C3)NC4=NC=CS4)C(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 92 mg/mL
(199.16 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Aurora A
(Cell-free assay) 0.064 nM
|
|---|---|
| In vitro |
MK-5108 hemmt die Aurora-A-Aktivität auf ATP-kompetitive Weise. Diese Verbindung zeigt in biochemischen Assays eine robuste Selektivität gegenüber den anderen Familienkinasen Aurora-B (220-fach) und Aurora-C (190-fach). Es zeigt auch eine hohe Selektivität für Aurora-A gegenüber anderen Proteinkinasen. Die Verbindung hemmt nur eine Kinase (TrkA) mit einer Selektivität von <100-fach. Es könnte selektiver für Aurora-A sein als MLN8054. Im Einklang mit der Induktion von pHH3-positiven Zellen induziert diese Chemikalie die Akkumulation von Zellen in der G2-M-Phase. Es hemmt die Proliferation von Tumorzellen, einschließlich HCC1143, AU565, MCF-7, HCC1806 und CAL85-1, mit einer IC50 von 0,42 μM, 0,45 μM, 0,52 μM, 0,56 μM bzw. 0,74 μM. Diese Verbindung verringert die Zellviabilität dosisabhängig in allen drei Zelllinien, einschließlich LEIO285-, LEIO505- und SK-LSM1-Zellen, mit einer IC50 von ungefähr 100 nM. Die Inkubation damit in LEIO285 erhöht den Anteil der Zellen in G2/M 48 und 72 Stunden nach der Behandlung. Die Verbindung erhöht die Caspase-3/7-Aktivität im Vergleich zu DMSO-behandelten Kontrollkulturen zu beiden Zeitpunkten signifikant. In LEIO505-Zellen führt sie zu einer stärkeren Akkumulation von Zellen in den G2/M-Phasen nach 24 Stunden, aber nicht nach 48 oder 72 Stunden. |
| Kinase-Assay |
Biochemische Kinase-Assays
|
|
Rekombinantes His-getaggtes humanes Aurora-A-Protein wird in Escherichia coli exprimiert und mit einer HisTrap HP-Säule gereinigt. Gereinigtes rekombinantes humanes Aurora-B- und Aurora-C-Protein wird käuflich erworben. Experimente werden in Fünffachbestimmung in 96-Well-Platten durchgeführt. Die Aurora-A-Assay-Reaktion wird in Gegenwart von 20 μM ATP, 25 μM Tetra-Kemptide [RRR(GLRRASLG)4R-NH2], 1,0 μCi pro Well [γ-33P]-ATP, 0,1 ng pro Well Aurora-A in 50 mM Tris-HCl (pH 7,4), 15 mM Mg(OAc)2 und 0,2 mM EDTA bei 30 °C für 40 Minuten durchgeführt. Um den Hemmmodus von MK-5108 für Aurora-A zu untersuchen, werden die IC50-Werte dieser Verbindung in Gegenwart unterschiedlicher ATP-Konzentrationen bestimmt. Dann wird der IC50-Wert als Funktion der ATP-Konzentration aufgetragen, um den Effekt der ATP-Konzentration auf den IC50-Wert dieser Chemikalie zu analysieren. Die Aurora-B-Assay-Reaktion wird in Gegenwart von 15 μM ATP, 100 μM Kemptide (GLRRASLG-NH2), 1,0 μCi pro Well [γ-33P]-ATP, 5,0 ng pro Well Aurora-B in 50 mM Tris-HCl (pH 7,4), 15 mM Mg(OAc)2 und 0,2 mM EDTA bei 30 °C für 20 Minuten durchgeführt. Die Aurora-C-Assay-Reaktion wird in Gegenwart von 40 μM ATP, 100 μM Kemptide, 1,0 μCi pro Well [γ-33P]-ATP, 15 ng pro Well Aurora-C in 10 mM MOPS-NaOH (pH 7,4), 5 mM Mg(OAc)2, 1 mM (±) DTT und 1 mM EGTA bei 30 °C für 20 Minuten durchgeführt. Nach Beendigung der Kinase-Reaktionen durch Zugabe von 2,0 % Phosphorsäure werden Tetra-Kemptide oder Kemptide auf der MultiScreen-PH-Platte eingefangen. Die Wells werden fünfmal mit 0,64 % Phosphorsäure gewaschen und dann auf Radioaktivität in einem Flüssigkeitsszintillationszähler überwacht.
|
|
| In vivo |
MK-5108 induziert pHH3-positive Zellen in Dosen von 16 mg/kg und 32 mg/kg. Die Plasmakonzentration dieser Verbindung bei 8 mg/kg und 16 mg/kg beträgt 1,7 μM bzw. 4,4 μM. Diese Verbindung führt zur Induktion von pHH3 in Tumor- und Hautgeweben, die nach 2 Stunden beginnt und nach 4 Stunden ein Maximum erreicht. Chemische Behandlungen mit 15 mg/kg und 30 mg/kg führen zu einer signifikanten Hemmung des Tumorwachstums mit einer Änderung des mittleren Tumorvolumens für die Behandlungsgruppe als Prozentsatz der mittleren Änderung in der Kontrollgruppe (%T/C) von 10 % und −6 % an Tag 11 bzw. 17 % und 5 % an Tag 18. Es wird bei beiden Dosen gut vertragen, mit minimaler Reduzierung des Körpergewichts. Diese Verbindung zeigt auch eine signifikante Antitumoraktivität durch intermittierende Dosierung bei nackten Ratten mit SW48-Tumoren, wobei 15 mg/kg und 45 mg/kg eine dosisabhängige Tumorwachstumshemmung mit einem %T/C von 35 % und 7 % an Tag 10 bzw. 58 % und 32 % an Tag 27 verursachen. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-Aurora A / Aurora-A / N-MYC |
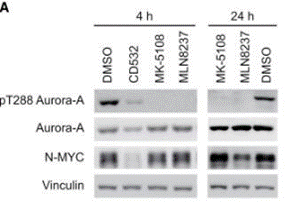
|
29262328 |
| Growth inhibition assay | Cell viability |
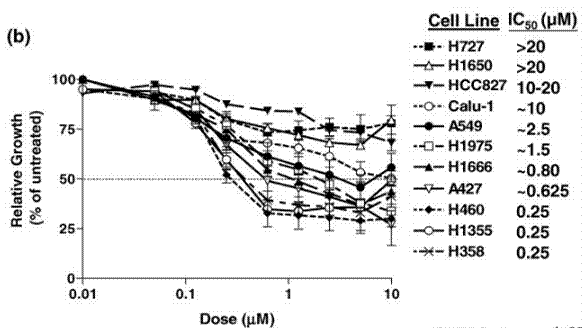
|
24756365 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
