nur für Forschungszwecke
Bestatin (Ubenimex) Immunology & Inflammation related Inhibitor
Kat.-Nr.S1591
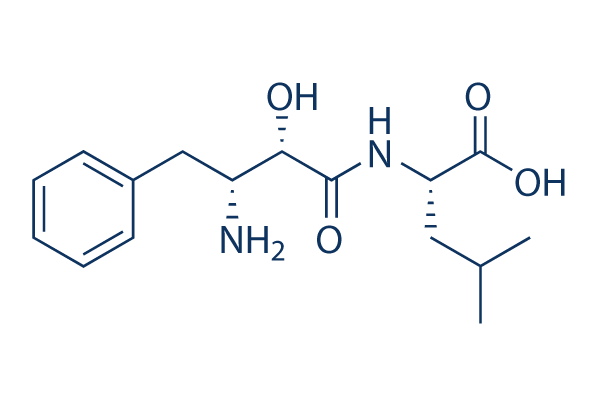
Chemische Struktur
Molekulargewicht: 308.37
Qualitätskontrolle
| Verwandte Ziele | PD-1/PD-L1 CXCR STING AhR CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Weitere Immunology & Inflammation related Inhibitoren | Cl-amidine Bindarit (AF 2838) Tranilast Tempol Sinomenine GI254023X (GI4023) ATP Geniposidic acid CORM-3 Oxymatrine |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 308.37 | Formel | C16H24N2O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 58970-76-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | NK421 | Smiles | CC(C)CC(C(=O)O)NC(=O)C(C(CC1=CC=CC=C1)N)O | ||
Löslichkeit
|
In vitro |
DMSO
: 7 mg/mL
(22.7 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Aminopeptidase-N
|
|---|---|
| In vitro |
Bestatin (Ubenimex) hemmt die Proliferation aller menschlichen Leukämiezelllinien außer KG1. Es induziert quantitativ die DNA-Fragmentierung und DNA-Leiter und erhöht die Caspase-3-Aktivität in U937-Zellen. Diese Verbindung induziert dosisabhängig die DNA-Fragmentierung in menschlichen Leukämiezelllinien. Es hemmt auch dosisabhängig die Invasion von SN12M-Zellen in rekonstituierte Basalmembran (Matrigel). Bestatin hemmt den Abbau von Kollagen Typ IV durch Tumorzellen, aber nicht durch Tumor-konditioniertes Medium (TCM), auf konzentrationsabhängige Weise. Es hemmt hydrolysierende Aktivitäten gegenüber Substraten von Aminopeptidasen in SN12M-Zellen. Die Verbindung hemmt die röhrenähnliche Bildung menschlicher Nabelschnurvenen-Endothelzellen (HUVECs) in vitro. Es übt eine direkte stimulierende Wirkung auf Lymphozyten (und Monozyten) über seine Fixierung an der zellulären Oberflächen-Leucin-Aminopeptidase aus, und eine indirekte Wirkung auf Monozyten (und Lymphozyten) über die Aminopeptidase-B-Hemmung des Tuftsin-Katabolismus. |
| In vivo |
Bestatin (Ubenimex) hemmt signifikant die durch Melanomzellen induzierte Angiogenese in einem Maus-Dorsal-Air-Sac-Assay und reduziert die Anzahl der Gefäße, die auf der dorsalen Seite von Mäusen, denen B16-BL6-Melanomzellen implantiert wurden, auf die etablierte primäre Tumormasse ausgerichtet sind. Es hemmt auch statistisch signifikant die Leukotrien-B4-Biosynthese in den Ösophagusgeweben von EGDA-Ratten und reduziert die Inzidenz von EAC von 57,7 % (15 von 26 Ratten) auf 26,1 % (6 von 23 Ratten). |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
