nur für Forschungszwecke
EED226 DNA/RNA Synthesis Inhibitor
Kat.-Nr.S8496
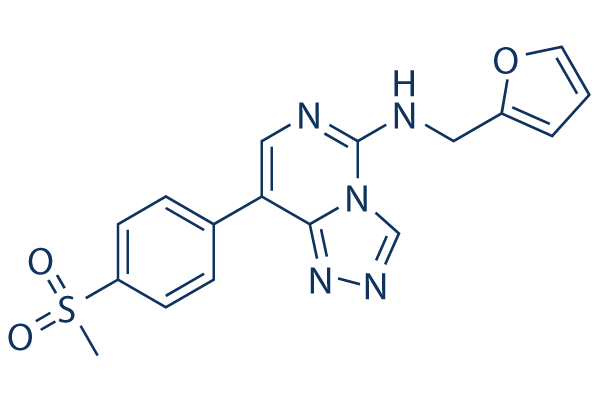
Chemische Struktur
Molekulargewicht: 369.40
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | HDAC JAK BET Histone Methyltransferase PKC PARP HIF PRMT EZH2 AMPK |
|---|---|
| Weitere DNA/RNA Synthesis Inhibitoren | CX-5461 (Pidnarulex) B02 SCR7 Favipiravir (T-705) RK-33 BMH-21 Triapine (3-AP) Carmofur YK-4-279 Halofuginone |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| KARPAS422 | Antiproliferative assay | up to 14 days | Antiproliferative activity against human KARPAS422 cells harboring monoallelic Y641N EZH2 mutation assessed as reduction in cell viability measured every 3 to 4 days up to 14 days by Beckman Coulter-based method, IC50 = 0.08 μM. | 28092155 | ||
| G401 | Function assay | 48 hrs | Inhibition of EED in human G401 cells assessed as reduction in global H3K27me3 level after 48 hrs by ELISA, IC50 = 0.22 μM. | 28092155 | ||
| KARPAS422 | Antitumor assay | 300 mg/kg | 34 days | Antitumor activity against human KARPAS422 cells xenografted in Balb/C nude mouse assessed as tumor regression at 300 mg/kg, po BID for 34 days | 28092155 | |
| KARPAS422 | Antitumor assay | 1.5 to 40 mg/kg | 2 weeks | Antitumor activity against human KARPAS422 cells xenografted in Balb/C nude mouse assessed as reduction in tumor volume at 1.5 to 40 mg/kg, po BID for 2 weeks | 28092155 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 369.40 | Formel | C17H15N5O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 2083627-02-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CS(=O)(=O)C1=CC=C(C=C1)C2=CN=C(N3C2=NN=C3)NCC4=CC=CO4 | ||
Löslichkeit
|
In vitro |
DMSO
: 73 mg/mL
(197.61 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
EED
82 nM(Kd)
PRC2
114 nM(Kd)
|
|---|---|
| In vitro |
EED226 induziert eine Konformationsänderung bei Bindung an EED, was zum Verlust der PRC2-Aktivität führt. Diese Verbindung hemmt auch effektiv PRC2, das ein mutiertes EZH2-Protein enthält, das gegen SAM-kompetitive Inhibitoren resistent ist. Es reguliert die Histon-H3K27-Methylierung und die PRC2-Zielgenexpression in Zellen. In den in vitro enzymatischen Assays hemmt diese Chemikalie PRC2 mit einer IC50 (halbmaximale Hemmkonzentration) von 23,4 nM, wenn das H3K27me0-Peptid als Substrat verwendet wird, und einer IC50 von 53,5 nM, wenn das Mononukleosom als Substrat verwendet wird, wobei das stimulierende H3K27me3 bei 1 × Kact (1,0 μM) hinzugefügt wird. Es ist nicht-kompetitiv sowohl mit SAM als auch mit dem Peptidsubstrat. Diese Verbindung band an EED und den PRC2-Komplex mit einer 1:1-Stöchiometrie und Kd von 82 nM bzw. 114 nM. Es stört den PRC2-Komplex nicht und könnte seine Bindungstasche auch bei einem an PRC2 gebundenen SAM-kompetitiven EZH2-Inhibitor noch besetzen. Diese Chemikalie zeigt eine bemerkenswerte Selektivität für den PRC2-Komplex gegenüber 21 anderen Proteinmethyltransferasen, Kinasen und anderen Proteinklassen. Die einzige andere Histone Methyltransferase, die durch sie gehemmt werden kann, ist der EZH1-PRC2-Komplex. Es führt mit mäßiger Permeabilität zu einer dosisabhängigen Abnahme sowohl der globalen H3K27me3- als auch der H3K27me2-Marker in G401-Zellen.
|
| In vivo |
Diese Verbindung induziert effektiv eine Tumorregression in einem Maus-Xenograft-Modell. Es in einer festen Dispersionsformulierung wird von Tieren gut vertragen. Diese Chemikalie zeigt in der Maus-Xenograph-Studie eine klare dosisabhängige Wirksamkeit. Es hemmt das Wachstum von Xenografts des diffus großzelligen B-Zell-Lymphoms (DLBCL) und reduziert die H3K27me3-Spiegel in ähnlichem Maße wie ein EZH2-Inhibitor. Es hat eine sehr geringe in vivo und in vitro Clearance und eine orale Bioverfügbarkeit von ca. 100 %, ein geringes Verteilungsvolumen (0,8 L/kg), eine vernünftige terminale t1/2 (2,2 h) und eine moderate Plasmaproteinbindung (PPB) (14,4 %). Seine Löslichkeit ist relativ gering und nur wenig abhängig vom pH-Wert des Mediums.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
