nur für Forschungszwecke
Eugenol Immunology & Inflammation related Chemikalie
Kat.-Nr.S4706
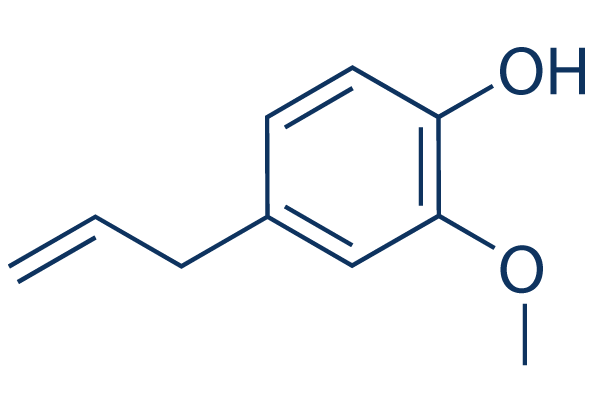
Chemische Struktur
Molekulargewicht: 164.20
Qualitätskontrolle
| Verwandte Ziele | PD-1/PD-L1 CXCR STING AhR CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Weitere Immunology & Inflammation related Inhibitoren | Cl-amidine Bestatin (Ubenimex) Bindarit (AF 2838) Tranilast Tempol Sinomenine GI254023X (GI4023) ATP Geniposidic acid CORM-3 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 164.20 | Formel | C10H12O2 |
Lagerung (Ab dem Eingangsdatum) | 2 years -20°C liquid |
|---|---|---|---|---|---|
| CAS-Nr. | 97-53-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
Löslichkeit
|
In vitro |
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Eugenol hat antiproliferative Wirkungen in verschiedenen Krebszelllinien sowie im B16-Melanom-Xenograftmodell. Es induziert Apoptose in verschiedenen Krebszellen, einschließlich Mastzellen, Melanomzellen und HL-60-Leukämiezellen. Diese Verbindung hat bei niedriger Dosis (2 μM) eine spezifische Toxizität gegen verschiedene Brustkrebszellen. Dieser tödliche Effekt wird hauptsächlich durch die Induktion des internen apoptotischen Signalwegs und eine starke Herunterregulierung von E2F1 und seines nachgeschalteten Anti-Apoptose-Ziels Survivin vermittelt, unabhängig vom Status von p53 und ERα. Es hemmt auch mehrere andere Brustkrebs-bezogene Onkogene, wie NF-κB und Cyclin D1. Darüber hinaus reguliert diese Chemikalie das vielseitige Cyclin-abhängige Kinase-Inhibitor-p21WAF1-Protein hoch und hemmt die Proliferation von Brustkrebszellen auf p53-unabhängige Weise.
|
|---|---|
| In vivo |
Eugenol hemmt die Proliferation von Brustkrebszellen auch in vivo. Die hemmende Wirkung dieser Verbindung auf Onkoproteine wird auch in vivo in Tumor-Xenografts beobachtet. Diese Chemikalie (0,2, 1,0, 5,0 oder 25 mg/kg), wenn sie oral zu drei verschiedenen Zeitpunkten in Bezug auf die CCl4-Dosis (i.p. Verabreichung von 0,4 mg/kg), d.h. vor (-1 Std.), gleichzeitig (0 Std.) oder nach (+ 3 Std.), verabreicht wird, verhindert signifikant den Anstieg der SGOT (Serum-Glutamat-Oxalacetat-Transaminase)-Aktivität, der Lipidperoxidation sowie der Lebernekrose. Die schützende Wirkung ist bei 1 mg und 5 mg Eugenol-Dosen deutlicher als bei 0,2 und 25 mg-Dosen. Die Abnahme der mikrosomalen G-6-pase-Aktivität durch CCl4-Behandlung wird jedoch durch diese Verbindung nicht verhindert, was darauf hindeutet, dass der Schaden am endoplasmatischen Retikulum nicht geschützt wird.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
