nur für Forschungszwecke
LCL161 IAP Inhibitor
Kat.-Nr.S7009
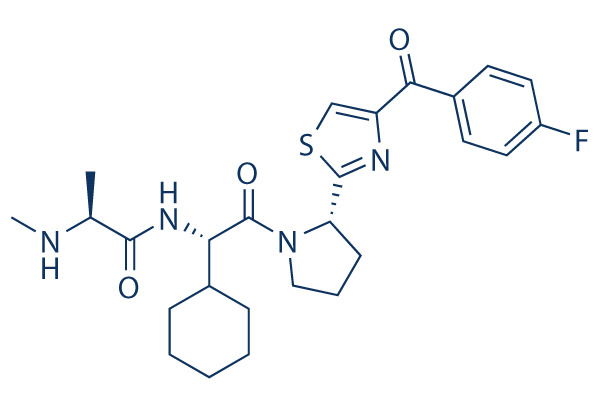
Chemische Struktur
Molekulargewicht: 500.63
Qualitätskontrolle
| Verwandte Ziele | Bcl-2 Caspase PD-1/PD-L1 Ferroptosis p53 Apoptosis related Synthetic Lethality STAT TNF-alpha Ras |
|---|---|
| Weitere IAP Inhibitoren | BV6 SM-164 Birinapant (TL32711) Xevinapant (AT406) GDC-0152 AZD5582 Tolinapant (ASTX660) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| LOX | Function assay | 100 mg/kg | 8 hrs | Potentiation of conatumumab-induced cIAP1 degradation in human LOX cells xenografted in mouse at 100 mg/kg, po after 8 hrs by Western blotting analysis | 24083782 | |
| LOX | Function assay | 8 hrs | Potentiation of conatumumab-induced caspase 3/7 activation in human LOX cells xenografted in mouse after 8 hrs by fluorescence assay | 24083782 | ||
| MDA-MB-231 | Function assay | 2.5 to 10 uM | 19 hrs | Binding affinity to cIAP1 BIR3 domain in human MDA-MB-231 cells assessed as increase in TNFalpha level at 2.5 to 10 uM after 19 hrs by ELISA | 24083782 | |
| BxPC3 | Function assay | 3.3 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human BxPC3 cells at 3.3 uM after 5 days by MTS assay | 24083782 | |
| HCT15 | Function assay | 3.3 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human HCT15 cells at 3.3 uM after 5 days by MTS assay | 24083782 | |
| SW620 | Function assay | 1.1 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human SW620 cells at 1.1 uM after 5 days by MTS assay | 24083782 | |
| SW620 | Function assay | 3.3 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human SW620 cells at 3.3 uM after 5 days by MTS assay | 24083782 | |
| LOX | Function assay | 3.3 uM | 3 days | Potentiation of conatumumab-induced cytotoxicity against human LOX cells at 3.3 uM after 3 days by MTS assay | 24083782 | |
| LS180 | Function assay | 3.3 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human LS180 cells at 3.3 uM after 5 days by MTS assay | 24083782 | |
| H460 | Function assay | 3.3 uM | 5 days | Potentiation of conatumumab-induced cytotoxicity against human H460 cells at 3.3 uM after 5 days by MTS assay | 24083782 | |
| LOX | Function assay | 100 mg/kg | 8 hrs | Plasma concentration in nude mouse xenografted with human LOX cells at 100 mg/kg, po measured at 8 hrs, Cp = 3.3 μM. | 24093940 | |
| SW620 | Function assay | 5 days | Induction of sensitization of human SW620 cells to conatumumab-induced apoptosis assessed as cell viability after 5 days by MTS assay, EC90 = 6.66 μM. | 24093940 | ||
| LOX | Function assay | 100 mg/kg | 8 hrs | Drug uptake in tumor of nude mouse xenografted with human LOX cells at 100 mg/kg, po measured at 8 hrs, Drug uptake = 18.4 μM. | 24093940 | |
| SW620 | Function assay | 2.5 uM | 5 days | Induction of sensitization of human SW620 cells to conatumumab-induced apoptosis assessed as cell viability at 2.5 uM after 5 days by MTS assay | 24093940 | |
| LOX | Function assay | 100 mg/kg | 8 hrs | In vivo inhibition of XIAP BIR2 domain in human LOX cells xenografted in nude mouse assessed as potentiation of conatumumab-induced caspase 3/7 activity at 100 mg/kg, po after 8 hrs by Western blot analysis | 24093940 | |
| LOX | Function assay | 100 mg/kg | 8 hrs | In vivo inhibition of XIAP BIR2 domain in human LOX cells xenografted in nude mouse assessed as increase in caspase 3/7 activity at 100 mg/kg, po after 8 hrs by Western blot analysis | 24093940 | |
| MDA-MB-231 | Function assay | 0.37 to 3.3 uM | 19 hrs | Inhibition of cIAP1/2 in human MDA-MB-231 cells assessed as induction of TNFalpha level at 0.37 to 3.3 uM after 19 hrs by ELISA | 24093940 | |
| CHL1 | Function assay | 0.4 to 10 uM | 28 hrs | Inhibition of cIAP1 in human CHL1 cells at 0.4 to 10 uM after 28 hrs by Western blot analysis | 24093940 | |
| SKMES1 | Function assay | 2.5 uM | 5 days | Potentiation of conatumumab-induced apoptosis in human SKMES1 cells at 2.5 uM after 5 days by MTS assay | 24093940 | |
| Capan1 | Function assay | 2.5 uM | 5 days | Potentiation of conatumumab-induced apoptosis in human Capan1 cells at 2.5 uM after 5 days by MTS assay | 24093940 | |
| AGS | Function assay | 2.5 uM | 5 days | Induction of sensitization of human AGS cells to conatumumab-induced apoptosis assessed as cell viability at 2.5 uM after 5 days by MTS assay | 24093940 | |
| U118MG | Function assay | 2.5 uM | 5 days | Potentiation of conatumumab-induced apoptosis in human U118MG cells at 2.5 uM after 5 days by MTS assay | 24093940 | |
| PC3 | Function assay | 2.5 uM | 5 days | Induction of sensitization of human PC3 cells to conatumumab-induced apoptosis assessed as cell viability at 2.5 uM after 5 days by MTS assay | 24093940 | |
| CCRF-CEM | Antiproliferative assay | Antiproliferative activity against human CCRF-CEM cells, GI50 = 0.25 μM. | 28435526 | |||
| MDA-MB-231 | Function assay | 2 hrs | Induction of cIAP1 degradation in human MDA-MB-231 cells after 2 hrs, EC50 = 0.0004 μM. | 28492317 | ||
| MDA-MB-231 | Cytotoxicity assay | 72 hrs | Cytotoxicity against human MDA-MB-231 cells assessed as decrease in cell proliferation after 72 hrs by alamar blue assay, EC50 = 0.0078 μM. | 28492317 | ||
| HEK293 | Function assay | 2 hrs | Inhibition of full length FLAG-tagged XIAP (unknown origin) interaction with full length untagged caspase-9 expressed in HEK293 cells after 2 hrs by immunoprecipitation assay, EC50 = 0.035 μM. | 28492317 | ||
| MDA-MB-231 | Antitumor assay | 30 mg/kg | 24 days | Antitumor activity against human MDA-MB-231 cells xenografted in Balb/c SCID mouse assessed as tumor growth inhibition at 30 mg/kg administered via oral gavage for 24 days | 28492317 | |
| MDA-MB-231 | Function assay | 2 hrs | Induction of intracellular cIAP1 degradation in human MDA-MB-231 cells after 2 hrs, IC50 = 0.0004 μM. | 30091600 | ||
| MDA-MB-231 | Antiproliferative assay | 72 hrs | Antiproliferative activity against human MDA-MB-231 cells after 72 hrs by Alamar blue assay, IC50 = 0.0078 μM. | 30091600 | ||
| HEK293 | Function assay | 2 hrs | Inhibition of full length FLAG-tagged XIAP (unknown origin) interaction with full length untagged caspase-9 expressed in HEK293 cells after 2 hrs by immunoprecipitation assay, IC50 = 0.035 μM. | 30091600 | ||
| SKOV3 | Apoptosis assay | 48 hrs | Induction of apoptosis in human SKOV3 cells assessed caspase-3 activation after 48 hrs by IncuCyte S3 live-cell analysis, EC50 = 0.001 μM. | 31095386 | ||
| SKOV3 | Apoptosis assay | 24 hrs | Induction of apoptosis in human SKOV3 cells assessed caspase-3 activation after 24 hrs by IncuCyte S3 live-cell analysis, EC50 = 0.003 μM. | 31095386 | ||
| BL21(DE3) | Function assay | 2 hrs | Displacement of biotinylated AVPF from N-terminal His tagged recombinant human XIAP-BIR3 domain (253 to 347 residues) expressed in Escherichia coli BL21(DE3) cells incubated for 2 hrs by DELFIA, IC50 = 0.048 μM. | 31095386 | ||
| BL21(DE3) | Function assay | 8 hrs | Displacement of biotinylated AVPF from N-terminal His tagged recombinant human XIAP-BIR3 domain (253 to 347 residues) expressed in Escherichia coli BL21(DE3) cells incubated for 8 hrs by DELFIA, IC50 = 0.053 μM. | 31095386 | ||
| A549 | Function assay | 1 uM | 3 hrs | Induction of cIAP2 degradation in human A549 cells assessed as reduction in cIAP2 protein level at 1 uM incubated for 3 hrs by Western blot analysis | 31550155 | |
| SK-MEL-28 | Function assay | 1 uM | 3 hrs | Induction of cIAP1 degradation in human SK-MEL-28 cells assessed as reduction in cIAP1 protein level at 1 uM incubated for 3 hrs by Western blot analysis | 31550155 | |
| SK-MEL-28 | Function assay | 1 uM | 3 hrs | Induction of cIAP2 degradation in human SK-MEL-28 cells assessed as reduction in cIAP2 protein level at 1 uM incubated for 3 hrs by Western blot analysis | 31550155 | |
| HEK293T | Function assay | 10 uM | 6 hrs | Covalent binding affinity to HA-BIR3 domain of XIAP (unknown origin) expressed in HEK293T cells assessed as increase in band intensity at 10 uM incubated for 6 hrs by Western blot analysis | 31550155 | |
| A549 | Function assay | 1 uM | 3 hrs | Induction of cIAP1 degradation in human A549 cells assessed as reduction in cIAP1 protein level at 1 uM incubated for 3 hrs by Western blot analysis | 31550155 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 500.63 | Formel | C26H33FN4O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1005342-46-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC(C(=O)NC(C1CCCCC1)C(=O)N2CCCC2C3=NC(=CS3)C(=O)C4=CC=C(C=C4)F)NC | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(199.74 mM)
Ethanol : 100 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
cIAP
XIAP
|
|---|---|
| In vitro |
LCL161 bindet mit hoher Affinität an Inhibitoren von Apoptoseproteinen (IAPs) und initiiert die Zerstörung von cIAP1 und cIAP2, was ferner die Apoptose über die Caspase-Aktivierung induziert. Diese Verbindung hemmt das Wachstum von FLT3-ITD-exprimierenden Zellen bei alleiniger Verabreichung bescheiden, mit einer IC50 im Bereich von ~0,5 μM (Ba/F3-FLT3-ITD-Zellen) bis ~4 μM (MOLM13-luc+-Zellen). Die Wirksamkeit dieses Wirkstoffs gegen die D835Y-Mutante wird als erheblich höher beobachtet, mit einer IC50 von ~50 nM, wenn er gegen Ba/F3-D835Y-Zellen getestet wird. Die Behandlung von MOLM13-luc+-Zellen mit einer Kombination dieser Verbindung und PKC412 führt zu einer signifikant stärkeren Abtötung von Zellen als jeder Wirkstoff allein, wobei die Calcusyn-Kombinationsindizes Synergie nahelegen. PKC412 und diese Chemikalie induzieren Apoptose von MOLM13-luc+-Zellen. Die Kombination von PKC412 und diesem Wirkstoff führt zu einer höheren Induktion der Apoptose als jeder Wirkstoff allein. Es ist in der Lage, die Stroma-vermittelte Rettung von mutant FLT3-exprimierenden Zellen durch positive Kombination mit PKC412 zu überwinden. Diese Verbindung hemmt das Wachstum von Ba/F3.p210-Zellen mit einer IC50 von ~100 nM. Es hat auch eine Aktivität gegen medikamentenresistente Zellen gezeigt, die Punktmutationen in den Zielproteinen exprimieren. Dieser Wirkstoff bei 1000 nM ist in der Lage, Ba/F3-abgeleitete Zelllinien, die Resistenz gegen PKC412 verleihen und FLT3-ITD mit Punktmutationen in der ATP-Bindetasche von FLT3 exprimieren, größtenteils oder vollständig abzutöten. Es zeigt auch Aktivität in Konzentrationen von 100 bis 1000 nM gegen Ba/F3-Zellen, die verschiedene exprimieren. Diese Verbindung wird gegen die 23 Zelllinien im Pediatric Preclinical Testing Program (PPTP) in vitro-Panel über 96 Stunden evaluiert. Sie erreicht eine 50%ige Wachstumshemmung bei nur 3 der 23 getesteten PPTP-Zelllinien bei einer Konzentration von 10 μM. Die drei Zelllinien umfassen zwei T-Zell-ALL-Zelllinien (COG-LL-317 und CCRF-CEM) und eine anaplastische großzellige Lymphomzelllinie (Karpas-299), wobei CCRF-CEM und Karpas-299 die niedrigsten relativen IC50-Werte (0,25 bzw. 1,6 μM) zeigen. Es zeigt immunmodulatorische Eigenschaften auf menschliche Immunsubpopulationen. T-Lymphozyten, die mit dieser Verbindung behandelt wurden, zeigen eine signifikant erhöhte Zytokinsekretion bei Aktivierung, mit geringem Einfluss auf das Überleben oder die Proliferation von CD4- und CD8-T-Zellen. Die Behandlung von peripheren Blutmononuklearzellen mit diesem Wirkstoff verbessert signifikant das Priming naiver T-Zellen mit synthetischen Peptiden in vitro. Myeloide dendritische Zellen erfahren eine phänotypische Reifung nach dieser Chemikalie und zeigen eine reduzierte Fähigkeit, einen Tumorantigen-basierten Impfstoff zu kreuzpräsentieren. Diese Effekte werden potenziell durch eine beobachtete Aktivierung der kanonischen und nicht-kanonischen NF-κB-Signalwege nach dieser Verbindung mit einer daraus resultierenden Hochregulierung anti-apoptotischer Moleküle vermittelt. |
| In vivo |
LCL161 verstärkt signifikant die Fähigkeit von PKC412, das Wachstum von Ba/F3-FLT3-ITD-luc+-Zellen in vivo zu hemmen. Diese Verbindung zeigt auch eine positive Kombination mit den Standard-Chemotherapeutika Ara-c und Doxorubicin gegen FLT3-ITD-exprimierende Zellen und gegen D835Y-exprimierende Zellen. Es wird ein additiver Effekt erzielt, indem beide Chemikalien bei der Unterdrückung des Leukämiewachstums kombiniert werden. Dieser Wirkstoff (100 mg/kg) verstärkt die In-vivo-Wirkungen von hohen bis moderaten Dosen auf die Leukämielast bei Mäusen. Diese Verbindung wird gegen die Pediatric Preclinical Testing Program (PPTP) in vivo-Panels (30 oder 75 mg/kg [solide Tumoren] oder 100 mg/kg [ALL]) zweimal wöchentlich oral verabreicht getestet. Es induziert signifikante Unterschiede in der EFS-Verteilung bei etwa einem Drittel der soliden Tumor-Xenografts (Osteosarkom und Glioblastom), jedoch nicht bei ALL-Xenografts. Es werden keine objektiven Tumorantworten beobachtet. In vivo zeigt diese Chemikalie eine begrenzte Einzelwirkstoffaktivität gegen die untersuchten pädiatrischen präklinischen Modelle. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | cIAP1 / cIAP2 / XIAP / surivivin |
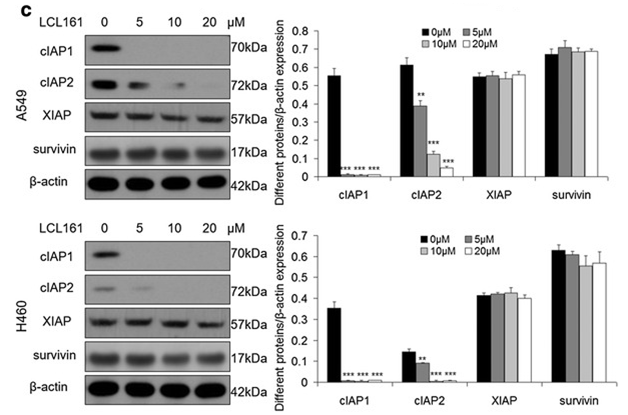
|
27737687 |
| Growth inhibition assay | Cell viability |
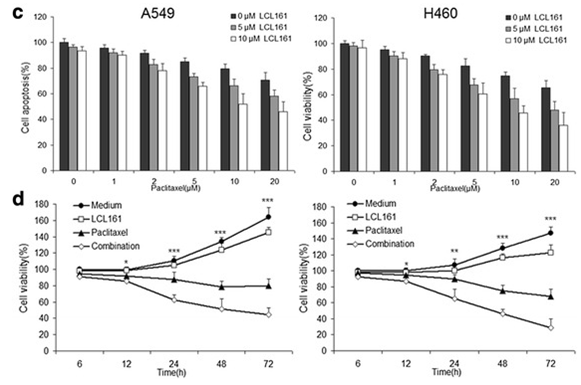
|
27737687 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03111992 | Completed | Multiple Myeloma |
Novartis Pharmaceuticals|Novartis |
December 18 2017 | Phase 1 |
| NCT01934634 | Unknown status | Metastatic Pancreatic Cancer |
US Oncology Research|Novartis Pharmaceuticals|Delta Clinical Research LLC |
March 2014 | Phase 1 |
| NCT01968915 | Completed | Neoplasms |
Novartis Pharmaceuticals|Novartis |
November 2013 | Phase 1 |
| NCT01617668 | Completed | Breast Cancer |
Novartis Pharmaceuticals|Novartis |
August 2012 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
