nur für Forschungszwecke
Sinomenine hydrochloride Immunology & Inflammation related Inhibitor
Kat.-Nr.S3758
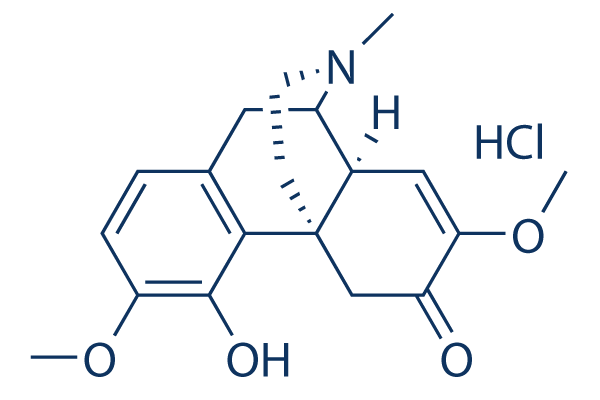
Chemische Struktur
Molekulargewicht: 365.85
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | PD-1/PD-L1 CXCR STING AhR CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Weitere Immunology & Inflammation related Inhibitoren | Cl-amidine Bestatin (Ubenimex) Bindarit (AF 2838) Tranilast Tempol Sinomenine GI254023X (GI4023) ATP Geniposidic acid CORM-3 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 365.85 | Formel | C19H23NO4.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 6080-33-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Cucoline hydrochloride, Kukoline hydrochloride, Sabianine A hydrochloride | Smiles | CN1CCC23CC(=O)C(=CC2C1CC4=C3C(=C(C=C4)OC)O)OC.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 73 mg/mL
(199.53 mM)
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Sinomenine induziert den apoptotischen Zelltod in U87-Zellen über die Aktivierung von Caspase-3, Caspase-8 und Caspase-9 sowie die Herunterregulierung von HIAP, Bcl-2 und Survivin. Sinomenine verringert die Expression von phosphoryliertem STAT3 (p-STAT3) sowohl in vivo als auch in vitro. Es hat vorteilhafte Rollen gegen verschiedene Arten von Krebs, einschließlich Brustkrebszellen, Ösophaguskarzinomzellen, hepatozellulären Karzinomzellen, Magenadenokarzinomzellen, Lungenkrebszellen und Dickdarmkarzinomzellen. Eine Behandlung mit Sinomenine führt zu einer dosis- und zeitabhängigen Wachstumshemmung bei U87, und die IC50 von SM lag zwischen 178 μM und 380 μM. Die Behandlung von U251, U373, Hs683 und T98G mit Sinomenine über 48 Stunden verringert die Zellviabilität offensichtlich, und die IC50 betragen 342,7 μM, 430,2 μM, 189,6 μM bzw. 270,3 μM. Sinomenine hydrochloride (SH) aktiviert einen Autophagy-vermittelten Zelltodweg, wie durch die akkumulierte Mikrotubuli-assoziierte Protein-Leichtkette 3B (LC3B)-II angezeigt, löst den autophagischen Fluss aus und verbessert die Zellviabilität nach Vorbehandlung mit Autophagy-Inhibitoren. Es induziert Autophagy, indem es den Akt-mTOR-Weg hemmt und den JNK-Weg aktiviert. Sinomenine hydrochloride (SH) reduziert dosisabhängig die Phosphorylierung von p70S6K, 4E-BP1, Akt und mTOR, während es die Expressionsniveaus der Autophagy-Markerproteine in vivo und in vitro erhöht. Sinomenine hydrochloride augmentiert dosisabhängig die ROS-Generierung, was mit einer erhöhten Autophagy in sowohl U87- als auch SF767-Zellen einhergeht. SH kann die lysosomale Biogenese durch Auslösen der nukleären Translokation von TFEB über die mTOR-Hemmung fördern.
|
|---|---|
| In vivo |
Sinomenine besitzt kardioprotektive, entzündungshemmende Aktivitäten und krebschemopräventive Eigenschaften. Es zeigt in vivo eine Anti-Gliom-Aktivität. Sinomenine wird von den Empfängermäusen in therapeutischer Dosis gut vertragen, und es treten keine signifikanten Zytotoxizitäten auf. Sinomenine hydrochloride (SH) initiiert den Autophagy-Lysosom-Weg sowohl in In-vitro- als auch in In-vivo-Experimenten.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
