nur für Forschungszwecke
Cisplatin DNA Synthesis Inhibitor
Kat.-Nr.S1166
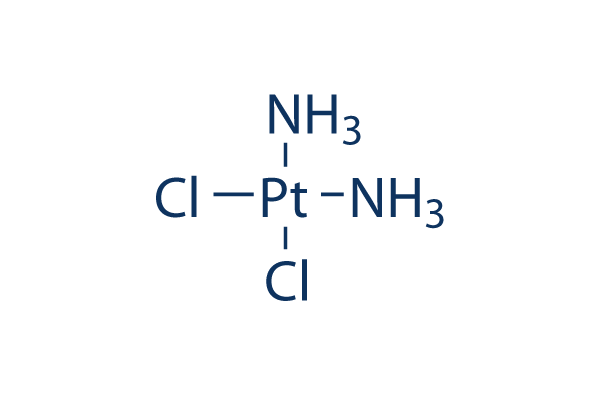
Chemische Struktur
Molekulargewicht: 300.05
Qualitätskontrolle
Produkte, die oft zusammen verwendet werden mit Cisplatin
| Verwandte Ziele | HDAC PARP ATM/ATR DNA-PK WRN Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere DNA/RNA Synthesis Inhibitoren | CX-5461 (Pidnarulex) B02 SCR7 Favipiravir (T-705) EED226 RK-33 BMH-21 Triapine (3-AP) Carmofur YK-4-279 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| Human osteosarcoma cells (HOS, 143B, U2OS and MG‑63) | Cell cycle analysis | 2 μM | 48 h | Cisplatin treatment markedly increased the G2/M population in all cell lines. | 31059083 | |
| OVC cells (A2780, TOV-112D, and cis-A2780) | Cell Cytotoxicity Assay | 0.5, 1, 2.5, 5, 10, 20, and 50 μM | 48 h | Combination of cisplatin and MEK inhibitor cobimetinib (10 nM) enhances cell death in three ovarian cancer cell lines (A2780, TOV-112D, and cis-A2780). | 31057611 | |
| HCC cell lines HepG2 and Huh7 | Cell viability assay | 0-30 μM | 48 h | CD133+ HCC cells exhibit resistance to cisplatin. | 31056532 | |
| Saos-2 cells | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | ||||
| OHS-50 cells | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | ||||
| SK-N-MC cells | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 300.05 | Formel | Cl2H6N2Pt |
Lagerung (Ab dem Eingangsdatum) | 2 years 4°C(in the dark) powder |
|---|---|---|---|---|---|
| CAS-Nr. | 15663-27-1 | SDF herunterladen | Lagerung von Stammlösungen | Lösungen sind instabil. Frisch zubereiten oder kleine, vorverpackte Größen kaufen. Nach Erhalt umpacken. | |
| Synonyme | NSC 119875, Cisplatinum, cis-diamminedichloroplatinum II, CDDP, cis DDP, DDP | Smiles | [NH2-].[NH2-].Cl[Pt+2]Cl | ||
Löslichkeit
|
In vitro |
DMF : 15 mg/mL Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
One of the most widely used and most potent chemotherapeutic agents. This product is not recommended to be dissolved in dimethylsulfoxide (DMSO).
|
|---|---|
| Targets/IC50/Ki |
DNA synthesis
(Tumor cells) |
| In vitro |
Cisplatin induziert Zytotoxizität durch Interaktion mit DNA zur Bildung von DNA-Addukten, die mehrere Signaltransduktionswege, einschließlich Erk, p53, p73 und MAPK, aktivieren, was in der Aktivierung der Apoptose gipfelt. Diese Verbindung (30 μM), 6 Stunden lang behandelt, induziert eine deutliche Aktivierung von Erk in HeLa-Zellen, die über die folgenden 14 Stunden anhält. Sie zeigt auch eine effektive antineoplastische Aktivität durch Induktion des Tumorzelltods. Sie zeigt die Fähigkeit, Apoptose von Nierenproximalkanaltubuluszellen (RPTC) zu verursachen, was zu Zellschrumpfung, einer 50-fachen Zunahme der Caspase-3-Aktivität, einer 4-fachen Zunahme der Phosphatidylserin-Externalisierung und einer 5- und 15-fachen Zunahme der Chromatin-Kondensation bzw. DNA-Hypoploidie führt. Diese Chemikalie (800 μM) verursacht nach 4 Stunden Behandlung typische Merkmale der Nekrose von RPTC. |
| In vivo |
Cisplatin hat sich als wirksam bei der Regression des Tumorwachstums in einer Vielzahl von Tiermodellen für Tumoren erwiesen, einschließlich Kopf- und Halskrebs-Xenografts, Zervix-Plattenepithelkarzinom-Xenografts, Hodenkarzinom-Xenografts, Ovarialkarzinom-Xenografts, Brustkarzinom-Xenografts, Dickdarmkarzinom, heterotransplantiertem Hepatoblastom und so weiter. Diese Verbindung (5 mg/kg) wurde wöchentlich i.v. am Tag 1 und 7 verabreicht und induzierte eine Tumorwachstumsinhibition (GI) von 77,5 % bzw. 85,1 % der serösen Xenografts Ov.Ri(C) und OVCAR-3. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | ATF3 FEN1 PD-L1 / p-MEK / MEK / p-STAT3 / STAT3 LC3B-I / LC3B-II / Beclin-1 p-AMPK / AMPK / p-mTOR / mTOR |
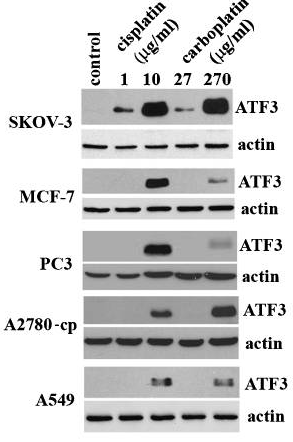
|
20651982 |
| Immunofluorescence | H2A.X / RPA γ-H2A.X / 53BP1 N-cadherin / E-cadherin / Vimentin LC3B |
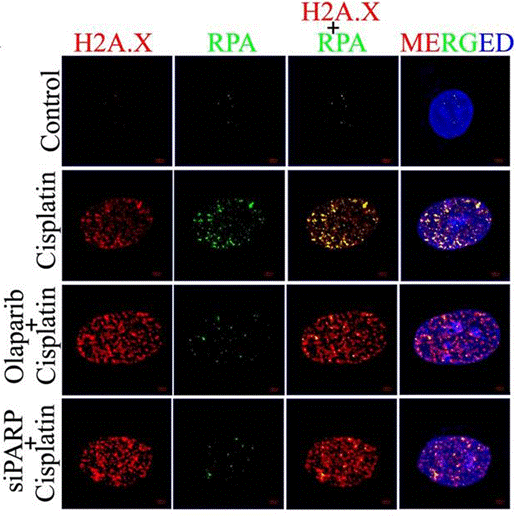
|
28993682 |
| Growth inhibition assay | Cell viability |
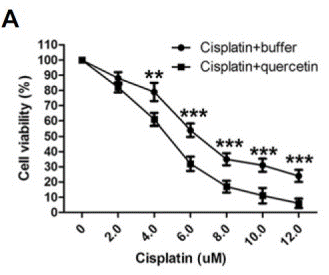
|
26062553 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06356155 | Not yet recruiting | Urothelial Carcinoma |
University of Michigan Rogel Cancer Center |
October 2024 | Phase 2 |
| NCT06393816 | Not yet recruiting | Large Cell Neuroendocrine Carcinoma of the Lung |
Centre Leon Berard|Groupe Français de Pneumo-Cancérologie |
May 2024 | Phase 2 |
| NCT06406465 | Not yet recruiting | Carcinoma Neuroendocrine|Tumor Neuroendocrine|Tumors Neuroendocrine|Neuroendocrine; Carcinoma|Small Cell; Receptors |
National Cancer Institute (NCI)|National Institutes of Health Clinical Center (CC) |
May 15 2024 | Phase 2 |
| NCT04915183 | Recruiting | Hearing Loss|Head and Neck Cancer |
National Institute on Deafness and Other Communication Disorders (NIDCD)|National Institutes of Health Clinical Center (CC) |
May 15 2024 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
What is the appropriate concentration of DMF for cell culture and animal study?
Antwort:
It depends on the cell type. The final concentration of DMF should be better limited to less than 0.1% if possible, or below 1%. Using saline as a vehicle for it at up to 3mg/ml is recommended. It's a suspension and can be administrated via oral gavage.
