nur für Forschungszwecke
RGFP966 HDAC3-Inhibitor
Kat.-Nr.S7229
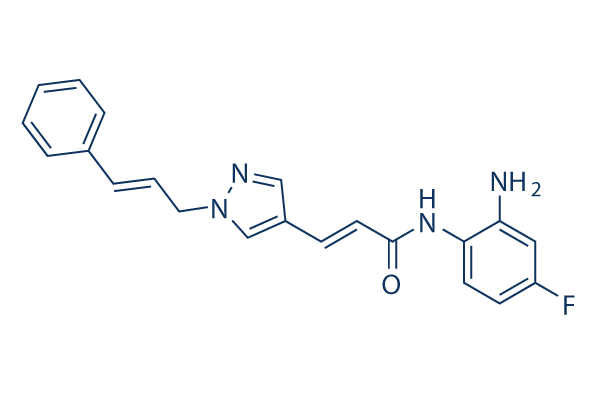
Chemische Struktur
Molekulargewicht: 362.4
Qualitätskontrolle
Produkte, die oft zusammen verwendet werden mit RGFP966
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| APL cells | Function assay | ≤2 μM | 48 h | DMSO | RGFP966 did not induce apoptosis in APL cells but did reduce clonogenicity and increased maturation. | 26447190 |
| Em-Myc lymphoma cells | Function assay | ≤1 μM | 48 h | DMSO | Cell proliferated significantly more slowly than vehicle-treated controls in the presence or absence of pro-survival BCL-2 overexpression | 26447190 |
| HH and Hut78 cells | Proliferation assay | 10 μM | 0, 24, 48, 72 h | DMSO | Both cell lines were sensitive to treatment with 10 μM 966. However, Hut78 cells exhibited a greater sensitivity than HH cells. | 23894374 |
| HH | Function assay | 10 μM | 24 h | DMSO | increases the acetylation at H3K9/K14, H3K27, and H4K5 | 23894374 |
| Hut78 | Function assay | 10 μM | 24 h | DMSO | increases the acetylation at H3K9/K14, H3K27, and H4K5 | 23894374 |
| HL60 | Antiproliferative assay | 48 hrs | Antiproliferative activity against human HL60 cells after 48 hrs in presence of JAK2 inhibitor CYT-387 by CCK-8 assay, IC50 = 1.64 μM. | 29940115 | ||
| K562 | Antiproliferative assay | 48 hrs | Antiproliferative activity against human K562 cells after 48 hrs in presence of JAK2 inhibitor CYT-387 by CCK-8 assay, IC50 = 1.64 μM. | 29940115 | ||
| HEL | Antiproliferative assay | 48 hrs | Antiproliferative activity against human HEL cells after 48 hrs in presence of JAK2 inhibitor CYT-387 by CCK-8 assay, IC50 = 1.64 μM. | 29940115 | ||
| HL60 | Antiproliferative assay | 48 hrs | Antiproliferative activity against human HL60 cells after 48 hrs by CCK-8 assay, IC50 = 21.71 μM. | 29940115 | ||
| K562 | Antiproliferative assay | 48 hrs | Antiproliferative activity against human K562 cells after 48 hrs by CCK-8 assay, IC50 = 21.71 μM. | 29940115 | ||
| HEL | Antiproliferative assay | 48 hrs | Antiproliferative activity against human HEL cells after 48 hrs by CCK-8 assay, IC50 = 21.71 μM. | 29940115 | ||
| Sf9 | Function assay | 60 mins | Inhibition of full length human C-terminal His-tagged HDAC3/N-terminal GST-tagged NCOR2 (395 to 489 residues) expressed in baculovirus infected Sf9 insect cells using substrate measured after 60 mins by colorimetric method | 29541372 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 362.4 | Formel | C21H19FN4O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1396841-57-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1=CC=C(C=C1)C=CCN2C=C(C=N2)C=CC(=O)NC3=C(C=C(C=C3)F)N | ||
Löslichkeit
|
In vitro |
DMSO
: 72 mg/mL
(198.67 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
HDAC3
(Cell-free assay) 80 nM
|
|---|---|
| In vitro |
RGFP966 ist ein langsam wirkender, kompetitiver, fest bindender HDAC-Inhibitor mit einer IC50 von 0,08 μM für HDAC3 und keiner effektiven Hemmung anderer HDACs bei Konzentrationen bis zu 15 μM. Die Behandlung von zwei CTCL-Zelllinien mit dieser Verbindung für 24 Stunden vor der Western-Blot-Analyse führte zu einer erhöhten Acetylierung an H3K9/K14, H3K27 und H4K5, aber nicht an H3K56ac. Es verringert das Zellwachstum in CTCL (kutanes T-Zell-Lymphom)-Zelllinien aufgrund erhöhter Apoptose, die mit DNA-Schäden und einer gestörten S-Phasen-Progression verbunden ist. Diese Chemikalie verursacht eine signifikante Reduzierung der Replikationsgabelgeschwindigkeit der DNA innerhalb der ersten Stunde der Arzneimittelbehandlung.
|
| Kinase-Assay |
Deacetylierungsassays
|
|
Deacetylierungsassays basieren auf dem homogenen Fluoreszenzfreisetzungsassay. Gereinigte rekombinante Enzyme werden mit seriell verdünnten Inhibitoren in den in den Abbildungen angegebenen Konzentrationen inkubiert, mit Präinkubationszeiten von 0 bis 3 Stunden, im Standard-HDAC-Puffer. Acetyl-Lys(Ac)-AMC-Substrat (bei 10 μM, entsprechend dem Km für sowohl HDAC1 als auch HDAC3) wird nach der Präinkubationszeit hinzugefügt. Die Reaktion läuft 1 Stunde lang. Der Trypsin-Peptidase-Entwickler in einer Endkonzentration von 5 mg/ml wird nach 1 Stunde hinzugefügt, und die Fluoreszenzemission wird dann mit einem Tecan M200 96-Well-Plattenlesegerät gemessen.
|
|
| In vivo |
RGFP966-Behandlung (10 mg/kg) verbessert das Langzeitgedächtnis für Objekterinnerungen. Diese Verbindung (3 oder 10 mg/kg, s.c.) erleichtert die Extinktion und verhindert die Wiederherstellung der Kokain-konditionierten Platzpräferenz.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-STAT3 / Acetyl-STAT3 / STAT3 / Ac-H3 / Ac-H4 H3K9K14ac / H3 / H3K56ac / H3K27ac / H4K5ac |
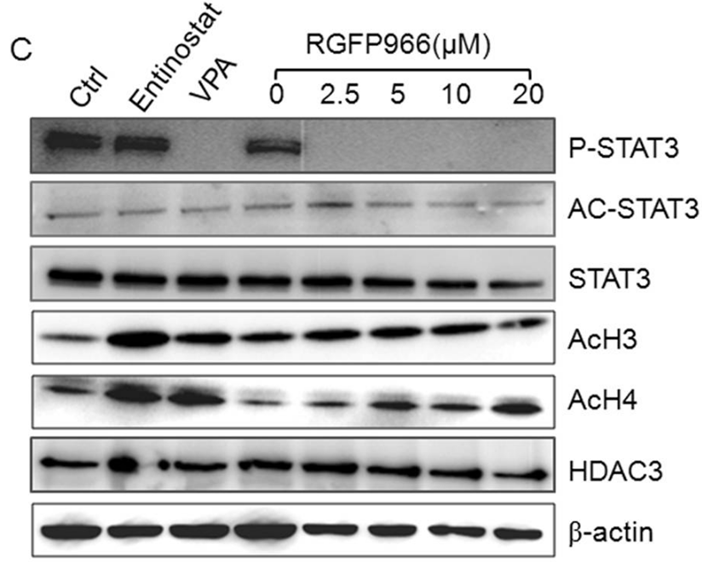
|
28338101 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
Does this product S7229 specifically inhibit HDAC3? Or does it target other HDACs as well?
Antwort:
In the paper, it is indicated that "this compound is specific for HDAC3, with an IC50 of 0.08 μM and no effective inhibition of any other HDAC at concentrations up to 15 μM." However, we did not perform experiment to confirm this data. Please refer to the following link for detailed information: http://www.pnas.org/content/110/7/2647.long
